Nos últimos 20 anos (a era da “sequenciação da próxima geração”: NGS em Inglês) foram feitos muitos esforços para avançar a nossa compreensão da genética do cancro. Infelizmente, embora seja agora possível mapear todas as mutações em pacientes com cancro, este esforço tecnológico não se traduziu no avanço esperado, nomeadamente na identificação de biomarcadores preditivos fiáveis ou na descoberta de novos alvos terapêuticos e de novas estratégias de tratamento.
De facto, embora o cancro seja uma doença genética (ou seja, que surge por defeitos genéticos), o seu estudo não deve centrar-se apenas nas células cancerígenas. É necessário estudar o contexto molecular e celular do cancro. Mas o que é que isto significa? Precisamos de decifrar o ambiente onde surgem e expandem as células cancerígenas: as células à sua volta, qual a sua função? Será que ajudam a progressão tumoral, ou pelo contrário tentam limitar a invasão do tecido saudável circundante? E as células cancerígenas próximas das células imunitárias, ou próximas dos vasos sanguíneos, terão as mesmas características (moleculares, genéticas), serão igualmente suscetíveis à terapia?
Todas estas questões só podem ser abordadas quando se olha diretamente e de forma detalhada para o tecido tumoral com o auxílio de microscópios com elevada resolução.
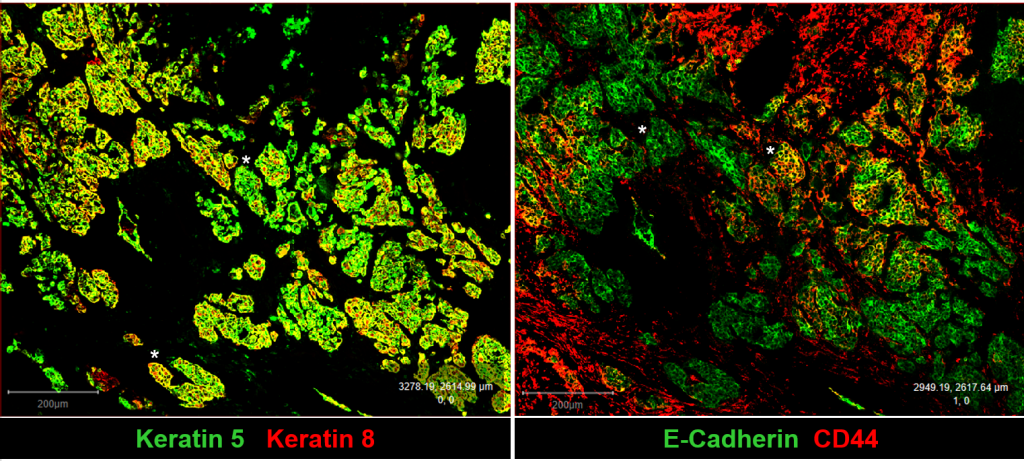
Apresentamos dois exemplos da heterogeneidade do tecido tumoral de cancro da mama, utilizando apenas dois marcadores por imagem: queratina 5 e queratina 8 à esquerda e E-caderina e CD44 à direita. As duas estrelas brancas em cada fotografia mostram uma acumulação de células cancerígenas “diferentes” dentro do mesmo tecido, indicando a variabilidade (diversidade) das células malignas.
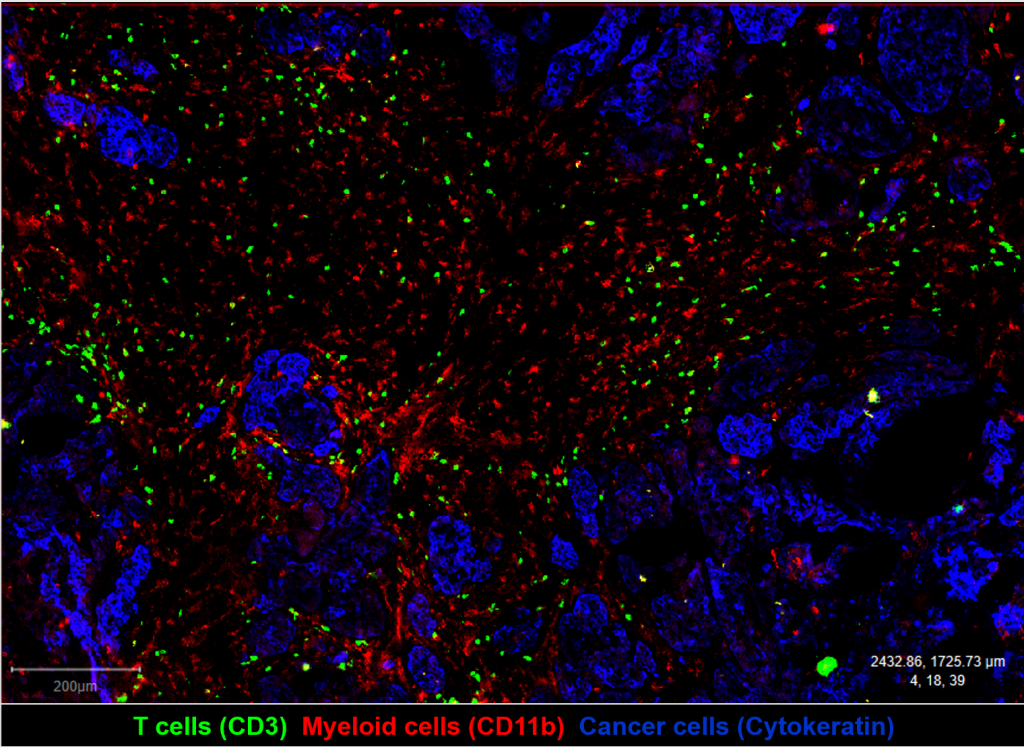
Depois, mostramos um exemplo de tecido tumoral de cancro da mama (corado a azul) altamente infiltrado com células imunitárias constituídas por linfócitos T (verde) e células mielóides (vermelho). Estas células podem ser manipuladas terapeuticamente (imunoterapia), pelo que é fundamental poder visualizá-las no tecido tumoral, e em particular perceber as suas interações com as células cancerígenas.
Acreditamos que o próximo passo em frente na compreensão da biologia do cancro virá com o desenvolvimento de técnicas que permitam a deteção de múltiplos marcadores nos próprios tecidos tumorais. A dissecção desta arquitetura do cancro poderá contribuir para a identificação de novos alvos com potencial terapêutico, bem como de biomarcadores que poderão estratificar (identificar) os doentes que poderão responder melhor às terapias existentes, nomeadamente a imunoterapia.

